Ювелирное обозрение
Все о ювелирных украшениях, драгоценных камнях и металлах
Как сделать простую батарейку
Содержание
- 1 Самодельная батарейка из подручных средств
- 2 Пошаговая инструкция по изготовлению батарейки
- 3 Необходимые материалы и инструменты
- 4 Зачистка шайб
- 5 Подготовка электролита
- 6 Работа с картоном
- 7 Растягивание трубки
- 8 Тестирование устройства
- 9 Итоговая сборка батарейки
- 10 Монтаж контактов
- 11 Способ первый: батарейка из лимона
- 12 Способ второй: банка с электролитом
- 13 Способ третий: медные монеты
- 14 Способ четвертый: батарейка в пивной банке
- 15 Способ пятый: картошка, соль и зубная паста
- 16 Как сделать аккумулятор своими руками
- 17 Как сделать мощный аккумулятор своими руками
- 18 Качественные системы зарядки Li-ion 18650
- 19 Самодельная батарейка из подручных средств
- 20 Видео
Батарейка является химическим источником электрического напряжения. Все имеющиеся в продаже элементы питания имеют похожие принципы действия. Положительный вывод изделия изготавливается из марганца или лития, отрицательный — из цинка или алюминия. Собрать батарейку своими руками можно из простых материалов.

Самодельная батарейка из подручных средств
Изготовить элемент питания можно из материалов, свойства которых похожи на характеристики используемых в промышленных условиях веществ.
Из лимона
В роли электролита выступает кислота, содержащаяся в соке фрукта. Электроды делают из тонкой проволоки, гвоздей или игл. Железный элемент является анодом, медный — катодом. Лимон разрезают пополам и помещают в небольшую емкость (банку или стакан). Провода соединяют с электродами, зачищенные концы вводят в мякоть фрукта на расстоянии 1 см друг от друга.
С помощью мультиметра измеряют напряжение, подаваемое самодельным гальваническим элементом. Если оно недостаточно высокое, несколько лимонных батарей соединяют последовательно.
Банка с электролитом
Используя этот метод, можно собрать устройство, напоминающее первый в мире аккумулятор. Электроды изготавливают из меди и алюминия. Элементы должны иметь большую площадь. Алюминиевый электрод соединяют с проводом с помощью зажима или болта, медный — припаивают. Детали погружают в банку на небольшом расстоянии друг от друга. Для фиксации применяют крышку с отверстиями. В качестве электролита используют такие составы:
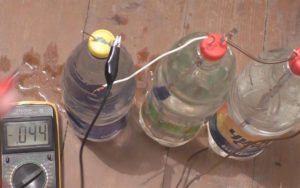
- Нашатырь. Вещество смешивается с водой в соотношении 1:2. Использовать нашатырный спирт в качестве электролита нельзя. Подходящее вещество (хлористый аммоний) имеет вид белого порошка без запаха. Его используют в качестве удобрения или флюса для пайки.
- Раствор серной кислоты. Вещество смешивают с водой в соотношении 1:5. Нельзя наливать кислоту первой. В таком случае добавляемая вода закипает, брызги попадают на кожу и одежду человека.
Раствор наливают в стеклянную емкость так, чтобы расстояние до краев банки составляло не менее 2 мм. С помощью мультиметра замеряют сопротивление и вычисляют нужное количество батарей. Принцип действия самодельного элемента сходен с таковым у солевого источника питания.
Медные монеты
Электроды изготавливают из алюминия и меди, в качестве электролита используют уксусную кислоту 9%. Монеты очищают от загрязнений, выдерживая в уксусе. Из картона и фольги вырезают кружки. Картонные изделия вымачивают в растворе уксусной кислоты, они должны впитать электролит. Из кружков и монет выкладывают столбик.
Первой кладется картонная деталь, второй — из фольги, третьей — монета. К крайним элементам заранее подсоединяют провода. Вместо пайки кабели можно прижать к металлическим деталям и заклеить скотчем. При эксплуатации батарейки монета становится непригодной. Не стоит изготавливать источники питания из ценных изделий.
Батарейка в пивной банке
Отрицательным выводом является корпус алюминиевой емкости, положительным — графитовый стержень. Также потребуются угольная пыль, пенопласт, вода, парафиновые свечи и соль. Верх банки снимают, из пенопласта вырезают кружок, который вставляют в емкость. Заранее проделывают отверстие для стержня. Последний устанавливают в центральной части банки. Оставшееся пространство заполняют угольной пылью. Материал пропитывают водным раствором соли (3 ст. л. продукта на 0,5 л воды). Края банки заливают парафином.
Картошка, соль и зубная паста
Батарейка из картошки предназначена для разового использования. Ее применяют для получения искры путем замыкания проводов. Для изготовления элемента потребуется крупная картофелина, изолированные медные кабели, соль, деревянные палочки и зубная паста. Сборку выполняют так:
- Картофель разрезают на 2 равные части. В одной половине формируют выемку, куда добавляют соль и пасту.
- Ингредиенты перемешивают до однородной консистенции. Электролит должен заполнить углубление.
- В другой половине картофелины проделывают 2 отверстия на расстоянии 1-2 см. Они должны совпасть с заполненным углублением.
- В отверстия вводят зачищенные концы проводов, половинки совмещают. Провода должны погрузиться в состав.
- Части картофеля закрепляют зубочистками. Через несколько минут кабели замыкают, высекая искру для разведения огня.
Пошаговая инструкция по изготовлению батарейки
Элементы питания цилиндрической формы высотой 50 мм легко изготавливаются в домашних условиях.
Необходимые материалы и инструменты
Перед началом опыта подготавливают такие материалы и инструменты:
- гофрированный картон;
- плоские шайбы из меди диаметром 1 см — 12 шт.;
- плоские шайбы из цинка диаметром 1 см — 15 шт.;
- очищенная вода;
- термоусадочная трубка;
- уксусная кислота 70%;
- поваренная соль;
- паяльник;
- емкости для приготовления растворов;
- мультиметр;
- наждачная бумага.
Зачистка шайб
В основе самодельного элемента питания лежит 11 медно-цинковых шайб, выдающих напряжение в 0,15 В. Детали должны участвовать в химических реакциях, поэтому их очищают наждачной бумагой. В результате получают ровную блестящую поверхность.
Подготовка электролита
Металлы создают электрический ток, однако для его проведения нужна среда. Электролит изготавливают из 120 мл воды, 4 ст. л. соли и 30 мл уксусной кислоты. Ингредиенты перемешивают и настаивают в течение часа.
Работа с картоном
Для формирования нужного расстояния между шайбами выкладывают кружки, вырезанные из гофрокартона. После нарезания материал пропитывают подготовленным на прошлом этапе раствором.
Растягивание трубки
Перед размещением медно-цинковых шайб трубке придают нужный диаметр. С помощью иглогубцев изделие растягивают на 10% от изначального размера.
Тестирование устройства
На медную шайбу накладывают пропитанный электролитом картон. Мультиметр переводят в режим постоянного напряжения. Черный провод подсоединяют к медной детали, красный — к цинковой. На экране прибора должно появиться значение 0,05-0,15 В. Этого достаточно для создании элемента питания из 11 токопроводящих компонентов.
Итоговая сборка батарейки
Элементы укладывают с соблюдением последовательности: медь — цинк — кусок картона. Каждую деталь выставляют перпендикулярно оси трубки. Для удобства шайбы вдавливают тонким стержнем. Установив последнюю деталь, самодельную батарейку сравнивают с заводской. При необходимости вводят дополнительную шайбу из цинка. Трубку прогревают, создавая подобие батарейки. Излишки удаляют.
Монтаж контактов
Прогретым паяльником приваривают к концам полученной конструкции точки из припоя. При установке в гнездо напаянные детали должны касаться контактов держателя батареи.
Батарейка или гальванический элемент – это химический источник электрического тока. Все батарейки, продающиеся в магазинах, по сути, имеют одинаковую конструкцию. В них используются два электрода из разного состава. Основным элементом для отрицательного вывода (анода) солевых и щелочных батареек является цинк, а для их положительного (катода) – марганец. Катод литиевых батареек изготавливается из лития, а для анода используются самые различные материалы.
Между электродами батареек расположен электролит. Состав его различен: для солевых батареек, имеющих самый низкий ресурс, используется хлорид аммония. Для изготовления щелочных батареек применяют гидроксид калия, а в литиевых батарейках используется органический электролит.
При взаимодействии электролита с анодом вблизи него образуется избыток электронов, создающий разность потенциалов между электродами. При замыкании электрической цепи количество электронов за счет химической реакции постоянно пополняется, и батарейка поддерживает протекание тока через нагрузку. При этом материал анода постепенно коррозирует и разрушается. При полной его выработке ресурс батарейки оказывается исчерпан.
Несмотря на то, что состав батареек сбалансирован производителями для обеспечения долгой и стабильной их работы, изготовить элемент питания можно и самому. Рассмотрим несколько способов, как можно сделать батарейку своими руками.
Способ первый: батарейка из лимона
Эта самодельная батарейка будет использовать электролит на основе лимонной кислоты, содержащаяся в мякоти лимона. Для электродов возьмем медную и железную проволочки, гвозди или булавки. Положительным будет медный электрод, а отрицательным – железный.
Лимон нужно разрезать поперек на две части. Для большей устойчивости половинки кладутся в небольшие емкости (стаканы или рюмки). Необходимо присоединить провода к электродам и погрузить их в лимон на расстоянии 0,5 – 1 см.
Теперь нужно взять мультиметр и измерить напряжение на получившемся гальваническом элементе. Если его недостаточно, то потребуется еще изготовить своими руками несколько одинаковых лимонных батареек и соединить их последовательно с помощью тех же проводов.
Способ второй: банка с электролитом
Для сборки своими руками устройства, похожего по конструкции на первую батарейку в мире, понадобится стеклянная банка или стакан. Для материала электродов используем цинк или алюминий (анод) и медь (катод). Для увеличения эффективности элемента их площадь должна быть максимально большой. Провода лучше будет припаять, но к электроду из алюминия провод придется прикрепить заклепкой или болтовым соединением, так как паять его сложно.
Электроды погружаются внутрь банки так, чтобы они не соприкасались друг с другом, и концы их находились выше уровня банки. Лучше их зафиксировать, установив распорку или крышку с прорезями.
Для электролита используем водный раствор нашатыря (50 г на 100 мл воды). Водный раствор аммиака (нашатырный спирт) – это не тот нашатырь, который используется для нашего опыта. Нашатырь (хлористый аммоний) – это порошок без запаха белого цвета, применяющийся при пайке в качестве флюса или как удобрение.
Второй вариант приготовления электролита – сделать 20% раствор серной кислоты. При этом нужно заливать кислоту в воду, и ни в коем случае не наоборот. Иначе вода мгновенно закипит и ее брызги вместе с кислотой попадут на одежду, лицо и глаза.
При работе с концентрированными кислотами рекомендуется надевать защитные очки и химически стойкие перчатки. Перед тем, как сделать батарейку с использованием серной кислоты, стоит подробнее изучить правила безопасности при работе с агрессивными веществами.
Осталось налить получившийся раствор в банку так, чтобы до краев сосуда оставалось не менее 2 мм свободного пространства. Затем при помощи тестера подобрать необходимое количество банок.
Собранный своими руками элемент питания похож по составу на солевую батарейку, так как содержит хлорид аммония и цинк.
Способ третий: медные монеты
Ингредиентами для изготовления такой батарейки своими руками являются:
- медные монеты;
- алюминиевая фольга;
- плотный картон;
- столовый уксус;
- провода.
Нетрудно догадаться, что электроды будут медные и алюминиевые, а в качестве электролита используется водный раствор уксусной кислоты.
Монеты для начала нужно очистить от окислов. Для этого их потребуется ненадолго опустить в уксус. Затем изготавливаем кружочки из картона и фольги по размеру монет, используя одну из них в качестве шаблона. Вырезаем кружки ножницами, картонные кладем на некоторое время в уксус: они должны пропитаться электролитом.
Затем из ингредиентов выкладываем столбик: сначала монету, затем – картонный кружок, кружок из фольги, снова монету и так далее, пока материал не иссякнет. Конечным элементом снова должна стать медная монета. К крайним монеткам можно заранее припаять провода. Если паять не хочется, то проводки прикладываются к ним, и вся конструкция плотно оборачивается скотчем.
В процессе работы этой батарейки, собранной своими руками, монеты придут в полную негодность, так что не стоит использовать нумизматический материал, представляющий культурную и материальную ценность.
Способ четвертый: батарейка в пивной банке
Анодом батарейки служит алюминиевый корпус банки из-под пива. Катодом – графитовый стержень.
- кусок пенопласта толщиной более 1 см;
- угольная крошка или пыль (можно применить то, что осталось от костра);
- вода и обычная поваренная соль;
- воск или парафин (можно использовать свечи).
От банки нужно отрезать верхнюю часть. Затем сделать кружок из пенопласта по размеру дна банки и вставить его внутрь, заранее сделав посередине отверстие для графитового стержня. Сам стержень вставляется в банку строго по центру, полость между ним и стенками заполняется угольной крошкой. Затем приготавливается водный раствор соли (на 500 мл воды 3 столовых ложки) и заливается в банку. Чтобы раствор не вылился, края банки заливаются воском или парафином.
Для подключения проводов к графитовым стержням можно использовать бельевые прищепки.
Способ пятый: картошка, соль и зубная паста
Такая батарейка – одноразового применения. Она годится для того, чтобы разжечь огонь, замкнув провода накоротко для получения искры.
Для создания картофельной зажигалки понадобится:
- большая картофелина;
- два медных провода в изоляции;
- зубочистки или похожие на них тонкие щепки;
- соль;
- зубная паста.
Разрезаем картофелину пополам так, чтобы плоскость разреза имела максимально возможную площадь. В одной половинке ножом или ложкой выбираем углубление, куда засыпаем соль и добавляем зубную пасту. Смешиваем их между собой до получения однородной массы. Количество «электролита» должно быть вровень с краями углубления.
В другой половинке, которая будет верхней, прокалываем два отверстия на некотором расстоянии между собой таким образом, чтобы они оба попали в углубление с электролитом при сборке «батарейки». В отверстие вставляем провода, предварительно зачищенные от изоляции примерно на сантиметр. Складываем половинки вместе так, чтобы концы проводов окунулись в электролит. Зубочистками скрепляем половинки между собой.
Ждем около пяти минут, после этого, замкнув провода между собой, можно высекать искру и разводить огонь.
Все описанные выше способы не являются полноценной заменой батарейки, купленной в магазине. Напряжение на самодельных элементах может колебаться и его величину невозможно точно подогнать. Долго пользоваться ими тоже не получится. Но где-нибудь в глуши при отсутствии электричества собрать своими руками элемент питания для мобильного телефона или светодиодной лампочки каждому вполне по силам. Естественно, при наличии соответствующих материалов под рукой.
Способы как сделать батарейку в домашних условиях – неплохая иллюстрация работы гальванических элементов. Сборка их своими руками доступна школьникам на уроках физики.
Всегда можно получить постоянное напряжение для питания небольших электронных устройств, если знать, как сделать аккумулятор своими руками. Аккумуляторы отличаются от батареек обратимостью своих химических реакций. Это значит, что они не только вырабатывают электрический ток и со временем разряжаются, а также обладают способностью восстанавливаться. Для этого нужно выполнить заряд, пропуская через аккумулятор ток от внешнего источника.

Как сделать аккумулятор своими руками
Химический источник тока (двухполюсник), способный после разряда восстанавливаться, можно выполнить своими руками. Любой химический источник тока, имеющий периодический режим работы (разряд – заряд), состоит из следующих основных элементов:
- электроды: анод и катод;
- электролит;
- разделительные пластины (сепараторы);
- корпус;
- контактные клеммы (выводы).
В качестве анода и катода используются различные пары химических элементов. Анод имеет отрицательный заряд – восстановитель, катод положительный заряд – окислитель.
Оба электрода погружены в электролит. Это водные растворы солей и кислот, проводящие электричество. Когда происходит разряд аккумулятора (двухполюсника) на нагрузку, анод окисляется и вырабатывает электроны, которые через электролит движутся к катоду. На катоде происходит процесс восстановления окислителя.
Важно! При работе на нагрузку ток через двухполюсник течёт от минуса к плюсу, при зарядке от постороннего источника тока (ИТ) – от плюса к минусу.
Для создания одной банки простейшего аккумулятора из меди и цинка понадобятся следующие детали:
- медная проволока длиной 100 мм;
- оцинкованная пластина размерами 25 * 50 мм;
- прокладка – вырезанная из москитной полиэтиленовой сетки полоска;
- электролит – соляной раствор;
- корпус из непрозрачного материала – герметичный стаканчик из-под кофе с крышкой.
Необходимо, чтобы ёмкость для аккумулятора была непрозрачной.
Сборка элемента производится в следующей последовательности:
- медная проволока скручивается спиралью, для увеличения площади рабочей поверхности к верхнему концу припаивается отвод;
- оцинкованная пластина также скручивается по окружности, к верхней части пластины припаивается отвод;
- в крышке баночки делается два отверстия для выводов: в центре – для медной проволоки и ближе к краю – для вывода цинкового электрода;
- медную спираль располагают по центру, вокруг неё размещают цинковую трубку, между ними вставляют изолирующую прокладку;
- заливают электролит: солёную воду (1л воды на 5 ст. л. соли) или уксус 15%;
- неплотно прикрывают крышку, предварительно продев в неё выводы.
К полученной банке подключают источник тока для зарядки самодельного аккумулятора. При этом нельзя плотно закрывать крышку. Или для выхода газов при заряде в ней проделывается множество мелких отверстий (кроме отверстий для выводов). У самодельного элемента плюс – на медном электроде, минус – на цинковом.
Внимание! Чем меньше расстояние между элементами меди и цинка, и чем больше площадь поверхности электродов, тем большее напряжение выдаст подобная аккумуляторная ячейка.
В идеале такой элемент вырабатывает 0,7 вольта. Недостаток такой АКБ заключается в высоком внутреннем сопротивлении и быстром саморазряде.
Как сделать мощный аккумулятор своими руками
Для того чтобы самодельный аккумулятор выдавал на выходе более 3,6 В постоянного тока, нужно собирать самодельные банки в последовательно соединённую батарею. Можно единичные элементы помещать в общий корпус.

Качественные системы зарядки Li-ion 18650
Литий-ионные источники электричества этого типа широко эксплуатируются с различными устройствами. Для их продолжительной работы необходима постоянная подзарядка. При заряде напряжение на элементе достигает значения 4,2 В, после чего снижается до 2-3 В. При глубоких разрядах (ниже 3 В) срок службы Li-ion 18650 значительно сокращается.

Важно! На долговечность влияет количество циклов «заряд-разряд». Это оптимальное число циклов, при которых ёмкость батареи при первом заряде (номинальная), отличается от текущей ёмкости после заряда не более, чем на 20%. Нормальным считается показатель – 350-500 циклов «заряд-разряд».
Существуют специальные зарядные устройства для подобных аккумуляторов, но их можно сделать самостоятельно, используя схему.

Регулировка тока осуществляется подбором резистора R4 на первоначальное значение тока зарядки. Он зависит от емкости аккумулятора. Например, если ёмкость батареи 3000 мА/ч, то ток зарядки равен 2-3 А.
Заводские системы контроля заряда самостоятельно делают регулировку этого параметра в рамках всего времени заряда.
Самодельная батарейка из подручных средств
Как можно сделать аккумуляторы, используя электролит и электроды, рассмотрено выше. Теперь о том, как быстро собрать источник тока однократного действия. Батарейка – это гальванический источник электричества, который не имеет способности восстанавливаться.
Способ первый: батарейка из лимона
Мякоть лимона содержит лимонную кислоту, она послужит электролитом. В качестве электрода выступают оцинкованный гвоздик и отрезок медной проволоки. Они втыкаются в лимон на расстоянии 50-100 мм друг от друга. Реакция окисления запускает движение электрического тока.

Способ второй: банка с электролитом
Литровую стеклянную банку используют в качестве ёмкости. В качестве электродов берутся цинковая и медная пластины. К пластинам прикрепляются провода, сами они опускаются в банку с электролитом. Им служит 20% раствор серной кислоты. Также можно использовать хлористый аммоний (нашатырь). На 100 мл воды берут 50 г. порошка. Уровень электролита не достигает края банки на 15-20 мм.

Осторожно! Работа с серной кислотой при приготовлении электролита подразумевает добавление воды в кислоту, а не наоборот. При приготовлении раствора необходимо использовать стеклянную посуду и стеклянную или деревянную палочку для перемешивания.
Способ третий: медные монеты
Принцип использования медного катода и алюминиевого анода рассмотрен в этом способе. Процесс изготовления источника тока следующий:
- по форме медных монет одного размера (медный пятак) вырезают кружочки из алюминиевой фольги и плотного картона (обложка старой книги);
- монеты очищаются путём погружения в уксус, им же пропитываются и кружочки картона;
- картон вставляется между монетой и кружком фольги, которые служат катодом и анодом.
Собранная таким образом батарея будет работать до тех пор, пока не высохнет электролит, пропитавший картонные кружки.

Способ четвертый: батарейка в пивной банке
Сам корпус пивной банки (алюминиевый) служит анодом (минус), в качестве катода используют графит. При изготовлении выполняются следующие шаги:
- удаляется верхняя часть банки;
- пенопластовый кружок диаметром, равным внутреннему диаметру банки, и толщиной не менее 10 мм укладывается на дно банки;
- в его центр вставляется графитовый стержень подходящего диаметра;
- свободное пространство между ним и стенками банки заполняется угольной крошкой;
- соляным раствором (5 ст. л. соли на 0,5 л воды) заполняется полученный элемент;
- верхняя часть устройства заливается расплавленным парафином или стеарином (от свечи);
- к стержню и корпусу банки с помощью зажимов «крокодил» присоединяются провода.

Способ пятый: батарейка из картошки
Это вариант использования химической реакции окисления между медными и оцинкованными полосками, в качестве электролита используется мякоть картофеля.
Внимание! Полученные напряжения таких источников настолько малы, что подобные конструкции могут служить лишь в качестве опытов для изучения происхождения электричества.

Способ шестой: графитовый стержень
Графитовый сердечник обматывается пористой фибровой салфеткой. Поверх него наматывается по спирали алюминиевая проволока. Вся конструкция опускается в подходящий по размеру стакан, заполненный «Белизной». Водный раствор хлорки служит электролитом.

Несмотря на всё разнообразие способов и видов самодельных источников тока, все они работают, благодаря электролитическим процессам и химическим реакциям окисления. Правильно подобранные пары элементов для анода и катода, а также использование подходящего электролитического раствора дают реальные результаты. Можно сделать аккумулятор своими руками для питания гаджетов и малогабаритных устройств.