Ювелирное обозрение
Все о ювелирных украшениях, драгоценных камнях и металлах
Какие металлы имеют металлический блеск

Металлы относятся к основным природным материалам используемым человечеством.
Металлургия – одна из базовых отраслей промышленности, определяющих экономический и военный потенциал страны. Создаются новые сплавы с заданными свойствами, в качестве добавок используются различные металлы.
Около 80% всех известных химических элементов ПСЭ составляют металлы. Наиболее распространенными металлами являются: Al – 8,8%; Fe – 4,0%; Ca – 3,6%; Na – 2,64%; K – 2,6%; Mg – 2,1%; Ti – 0,64%.
Для металлов характерны свой специфические свойства, отличающие их от металлоидов: пластичность, высокая тепло – и электропроводность, твердость, для большинства металлов высокая температура плавления и кипения, металлический блеск.
Пластичностью называется способность металлов под действием внешних сил подвергаться деформации, которая остается и после прекращения этого действия. Благодаря пластичности металлы подвергаются ковке, прокатке, штамповке. Металлы имеют различную пластичность.
Металлический блеск. Гладкая поверхность металлов отражает световые лучи. Чем меньше она эти лучи поглощает, тем больше металлический блеск. По блеску металлы можно расположить в следующий ряд: Ag, Pd, Cu, Au, Al, Fe.
На этом свойстве металлов основано производство зеркал.
Металлы характеризуются также высокой тепло – и электропроводностью. По электропроводности I место занимает Ag, Cu, Al.
С повышением температуры электропроводность уменьшается, так как усиливается колебательное движение ионов в узлах кристаллической решетки, что препятствует направленному движению электронов.
С понижением температуры электропроводность увеличивается и в области близкой к абсолютному нулю у многих металлов наблюдается сверхпроводимость.
Причиной общности физических и химических свойств металлов объясняется общностью строения их атомов и природой кристаллических решеток металлов.
Атомы металлов имеют большее, по сравнению с неметаллами размеры. Внешние электроны атомов металлов значительно удалены от ядра и связаны с ним слабо, поэтому металлы имеют низкие потенциалы ионизации (являются восстановителями).
Специфические свойства металлов – пластичность, тепло – и электропроводность, блеск объясняются тем, что в металлах имеются «свободные» электроны, способные перемещаться по всему кристаллу.
Для металлов характерна металлическая связь (она объясняется на основе метода МО).
Физические свойства металлов.
Все металлы, за исключением ртути, при обыкновенной температуре являются твердыми веществами с характерным металлическим блеском.
Большинство металлов имеют цвет от темно-серого, до серебристо-белого. Золото и цезий имеют желтый цвет, совершенно чистая медь – светло-розовый, некоторые металлы обладают красноватым оттенком (висмут).
Плотность металлов может колебаться в широких пределах; например плотность Li = 0,53г/см3 (самый легкий), а Os является самым тяжелым металлом 22,48г/см3.
В пределах одной подгруппы аналогов величины плотностей, как правило, растут с возрастанием заряда ядра атома.
В технике металлы классифицируются по плотности: легкие, тяжелые, легкоплавкие и тугоплавкие.
Нахождение в природе.
В природе металлы встречаются как в самородном состоянии, так и в виде различных соединений. В самородном состоянии находятся только химически малоактивные металлы – Pt, Ag, Au. Химически активные металлы встречаются только в виде различных соединений – руд.
Руды бывают: окисные, сульфидные и соли.
Предварительно руду обогащают, то есть отделяют от пустой породы. Самый распространенный метод – флотационный, он основан на различной смачиваемости поверхности минералов водой.
Методы извлечения минералов из руд определяются их химическим составом. Все способы получения металлов сводятся к реакциям окисления – восстановления.
Карботермия. В этом методе получения металлов восстановителем служит углерод – самый дешевый и самый доступный. Углерод применяют в виде кокса, а окисленный углерод легко удаляется в виде СО2.
Углерод применяется для восстановления сравнительно малоактивных металлов: Fe, Cu, Zn, Pb.
При восстановлении углеродом смеси железной руды с оксидами Cr, Mo, W или Mn в промышленности получают сплавы, содержащие примерно 70% указанных металлов и очень небольшое количество углерода. Это ферросплавы, служат для получения специальных легированных сталей. Для восстановления углеродом пригодны только окиси.
Сульфидные руды (цинковые, свинцовые, медные) сначала подвергают окислительному прокаливанию:
2ZnS + 2O2 → 2ZnO + SO2
Li, Ca, Ba также, как и металлы III группы, не могут быть получены восстановлением углеродом, так как они сразу же после выделения в свободном состоянии с избытком углерода образуют карбиды.
Металлотермия. Основана на процессах вытеснения одного металла (менее активного) другим (более активным) из соответствующих окислов, хлоридов, сульфидов.
Очень хорошим восстановителем окислов металлов вследствие большого сродства к кислороду является алюминий. Процесс называется алюминотермия.
Fe2O3 + 2Al = Al2O3 + 2Fe
Алюминотермией получают и другие металлы (Mn, Cr, Ti), которые не могут быть получены в чистом виде восстановлением их окисей углем из-за образования карбидов. В алюмотермической реакции выделяется большое количество тепла за очень короткое время, вследствие чего развивается высокая температура.
Электролитическое или катодное восстановление металлов. Для трудновосстанавливаемых металлов уголь как восстановитель непригоден и в этом случае применяют катодное восстановление, то есть выделение путем электролиза. Такие металлы могут окисляться водой, поэтому их соединения подвергаются электролизу не в водных растворах, а в расплавах или растворах других растворителей.
Например, металлические Na, K, Ba, Ca, Mg, Be получают электролизом расплавов соответствующих хлоридов.
Получение металлов высокой чистоты.
В связи с бурным развитием техники потребовались металлы, обладающие очень высокой чистотой. Например, для надежной работы ядерного реактора необходимо, чтобы в расщепляющихся материалах такие примеси как бор, кадмий и др., содержались в количестве, не превышающих миллионных долей процента. Чистый цирконий – один из лучших конструкционных материалов для атомных реакторов – становится совершенно непригодным для этой цели, если в нем содержится даже ничтожная примесь гафния.
Перегонка в вакууме. Этот метод основан на различной летучести очищаемого металла и имеющихся в нем примесей. Исходный металл загружается в специальный сосуд, соединенный с вакуумным насосом и в сосуде создают вакуум, после чего нижняя часть сосуда нагревается. На холодных частях сосуда осаждаются либо примеси, либо чистый металл, в зависимости от того, что является более летучим.
1. Карбонильный процесс. Этот процесс используют в основном для получения чистого никеля и чистого железа. Металл содержащий примеси, нагревают в присутствии СО (окиси углерода) и получающийся летучий карбонил отгоняют от нелетучих примесей. Затем карбонилы разлагают при более высоких температурах с образованием высокочистых металлов.
2. Йодистый процесс дает возможность получать такие металлы, как цирконий, титан.
3. Очистка металла (обычно содержащего в качестве примесей окисел) в вакууме при нагревании его до очень высокой температуры при помощи электрической дуги.
Зонная плавка. Этот метод заключается в протягивании бруска неочищенного Германия через узкую печь; образующаяся при этом расплавленная зона, по мере продвижения бруска через нее перемещается вдоль него и уносит за собой примеси.
Многократным повторением этого процесса можно достигнуть высокой степени чистоты.
Химические свойства металлов.
У металлов отсутствует способность присоединять электроны, следовательно металлы являются восстановителями. Мерой химической активности металлов является энергия ионизации J.
Окислителями металлов могут быть: элементарные вещества, кислоты, соли менее активных металлов и т. д.
1. Взаимодействие с элементарными веществами.
2. Взаимодействие с кислотами:
а) Окислитель – ион Н+ (HCl, H2SO4 (разб.) и т. д.);
б) Окислитель анион кислоты (к таким кислотам относятся HNO3 и H2SO4 (конц.);
в) Взаимодействие с водой;
г) Взаимодействие со щелочами;
д) Взаимодействие с растворами солей.
Все атомы кислорода непосредственно связаны с атомами металла и не связаны друг с другом: Ме * О2.
Классификация оксидов металлов
Основные – оксиды наиболее активных металлов (s – элементы I и II групп) – связь ионная: Na2O, K2O, CaO, MgO и т. д.
Их свойства: а) взаимодействуют с кислотами; б) с кислотными оксидами; в) с водой.
Амфотерные оксиды (менее активных металлов и d – элементов): Al2O3, ZnO, Cr2O3 и т. д.
Их свойства: а) взаимодействие с кислотами; б) взаимодействие со щелочами.
Кислотные – оксида малоактивных металлов в высших степенях окисления (CrO3, Mn2O7 и др.). Их свойства: а) взаимодействие с водой, образуя кислоты; б) взаимодействуют с основаниями (щелочами).
Характер изменения свойств оксидов
В пределах одного периода происходит ослабление основных свойств через амфотерные и усиление кислотных слева на право.
В группе у одного и того же элемента наблюдается такое же изменение свойств.
1. Непосредственное окисление металлов – горение.
2. Окисление сульфидов.
ZnS + O2 = ZnO + SO2
3. Окисление оксидами других элементов, если теплота образования получающегося оксида больше теплоты образования исходного (металлотермия).
Al + Cr2O3 = Cr + Al2O3 + Q
4. Обезвоживание соответствующих гидроксидов.
Al(OH)3  Al2O3 + H2O
Al2O3 + H2O
5. Термическое разложение карбонатов, нитратов, сульфатов и других солей.
СаСО3  СаО + СО2
СаО + СО2
Классификация: основные, амфотерные, кислотные (соответствуют оксидам).
Характер изменения свойств в природе – аналогично оксидам.
Характерный металлический блеск
Железо, медь и алюминий имеют характерный металлический блеск . [16]
Изучая твердые вещества, не имеющие характерного металлического блеска , мы замечаем, что их электропроводность очень низкая. К ним относятся вещества, которые мы называем ионными – хлористый натрий, хлористый кальций, нитрат серебра и хлористое серебро, а также молекулярные кристаллы, например лед. Лед, изображенный на рис. 5 – 3, состоит из тех же молекул, которые существуют в газовой фазе, но упорядочение расположенных в кристаллической решетке. Эти плохие проводники электрического тока сильно отличаются от металлов почти по всем свойствам. Таким образом, электропроводность может быть использована для классификации веществ, которая является однош из наиболее обоснованных. [17]
Металлами называются простые кристаллические вещества, имеющие характерный металлический блеск , хорошо проводящие тепло и электрический ток, способные изменять свою форму под действием внешних усилий и сохранять ее после снятия нагрузки без каких-либо признаков разрушения. Из всего количества химических элементов, известных в настоящее время, восемьдесят элементов относятся к металлам. Наиболее распространенными в земной коре металлами в виде химических соединений являются алюминий, железо, магний, калий, натрий и кальций. Чистые металлы имеют ограниченное применение в технике, так как в природе встречаются крайне редко, а получение их из химических соединений ( руд) связано с большими трудностями. [18]
В результате водородной коррозии поверхность стали теряет характерный металлический блеск и становится матовой. [20]
Полимеры представляют собой тонкодисперсные окрашенные порошки с характерным металлическим блеском , растворимые лишь в концентрированной серной кислоте. [21]
Все d – элементы являются металлами с характерным металлическим блеском . По сравнению с s – металлами их прочность значительно выше. [22]
Не растворившийся иод образует хорошо видимую пленку с характерным металлическим блеском ( плавающую на поверхности раствора) или собирается на дне колбы в виде черных частичек. Так как раствор иода окрашен в интенсивно красный цвет и почти не прозрачен, рассматривать его нужно очень тщательно, держа колбу против яркой электрической лампы, висящей на потолке. Для этого нужно встать под лампой, держа колбу за горло в наклонном положении между лампой и лицом, и стараться увидеть в ней яркое изображение лампы. На таком фоне не растворившиеся кристаллы иода хорошо заметны. Тогда кристаллы обоих веществ соберутся в одном месте и вокруг кристаллов иода создастся зона концентрированного раствора KJ, в котором иод быстро растворится. [23]
Все щелочные металлы – вещества серебристо-белого цвета, с характерным металлическим блеском , хорошей электро – и теплопроводностью, низкими температурами плавления и сравнительно низкими температурами кипения, малой плотностью и большим объемом атомов. В парообразном состоянии их молекулы одноатомны; ионы бесцветны. [25]
По внешнему виду темно-фиолетовые, почти черные кристаллы с характерным металлическим блеском . Хорошо растворяется в воде. Марганцовокислый калий относится к числу сильных окислителей, чем и обусловлены его дезинфекционные свойства. [26]
Благодаря коллективизированным электронам металлы обладают электро – и теплопроводностью, характерным металлическим блеском и некоторыми другими чисто металлическими свойствами. Например, блеск объясняется отражением световых лучей от коллективизированных электронов. [28]
Графит имеет цвет от серебристо-серого и темно-свинцового до черного с характерным металлическим блеском . [29]
Металлами называются химические элементы, отличительными признаками которых являются непрозрачность, характерный металлический блеск , свойство коваться, вытягиваться в нить и проволоку, свариваться, хорошо проводить тепло и электричество. Химические элементы, не обладающие перечисленными свойствами, называются неметаллами. [30]
Металлами называют вещества, обладающие своеобразным металлическим блеском, пластичностью, высокой прочностью, электро- и теплопроводностью, ковкостью и свариваемостью, что обусловлено особой природой металлической связи. У металлов своеобразные не только физические, но и химические свойства: способность к окислению и восстановлению в реакциях.
Большинство химических элементов (82 из 109- 75%) относится к металлам.
Свойства сплавов обычно резко отличаются от свойств исходных металлов и их можно регулировать.
Содержание химических элементов в земной коре колеблется в больших пределах. Наиболее распространенными и ценными являются:
Содержание остальных металлов составляет около 2%. Ряд металлов (цинк, олово, свинец, кобальт, вольфрам, молибден, ванадий) содержатся в тысячных долях процента, но имеют большое значение для получения высококачественных сплавов.
Характерная особенность строения металлов – наличие металлической связи между атомами. Атомы металлов на внешней оболочке содержат небольшое количество слабосвязанных электронов. Электронные облака атомов перекрываются, поэтому внешние электроны могут свободно перемещаться и являются как бы общими, не связанными с отдельными атомами. Таким образом, общие электроны образуют электронный газ, который свободно перемещается между ионами и скрепляет их друг с другом. Эта особенность определяет стремление атомов металла располагаться как можно плотнее. Компактная упаковка атомов приводит к повышенной плотности металлов.
Металлы и сплавы в твердом состоянии имеют кристаллическое строение, которое характеризуется определенным, закономерным расположением атомов. Атомы в кристалле металла образуют пространственно кристаллическую решетку, состоящую из многократно повторяющихся ячеек, имеющих относительно простую форму.
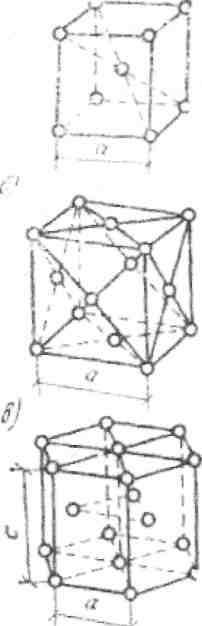
В промышленных металлах наиболее распространены следующие кристаллические решетки (рис. 1): кубическая объемно-центрированная, кубическая гранецентрированная и гексагональная. В элементарной кубической объемно-центрированной решетке находится девять атомов (восемь в вершинах куба и один в центре).
Такую решетку имеют: железо при температуре до 910 °С и выше 1390 °С, хром, вольфрам, ванадий и др. В кубической гранецентрированной решетке 14 атомов (восемь в вершинах куба и по одному в центре каждой грани). Такую решетку имеют: железо при температуре 910-1390 °С, медь, никель, алюминий и др. В гексагональной решетке,имеющей форму шестигранной призмы, 17 атомов (12 в вершинах, два в центре оснований и три внутри призмы). Данная решетка имеется у магния, цинка и других металлов.
Возможны и другие формы кристаллических решеток. Атомы в решетке находятся на определенных расстояниях один от другого. Эти расстояния очень малы и вычисляются в нанометрах (1 нм = 10" м). Расположение атомов, межатомные расстояния, насыщенность атомами – все это влияет на качество металлов.
Размеры кристаллической решетки характеризуются параметрами (периодами) — расстояниями между центрами атомов, расположенных в узлах элементарной ячейки. Например, для железа эти параметры равны 28,4-36,3 нм.
 |
 |
 |
 |
Рис. 1. Основные виды элементарных ячеек кристаллических решеток металлов а – объемно-центрированная кубическая; б – гранецентрированная кубическая; в – гексагональная плотноупакованная
При этом плотность и степень упаковки атомов кристаллической решетки характеризуется отношением бесчисленного множества кристаллических образований, группирующихся в виде отдельных прочно связанных между собой зерен. Большинство их имеет кубическую объемно-центрированную (хром, ванадий, молибден, вольфрам и некоторые другие) и кубическую гранецентриро-ванную решетки (алюминий, медь, никель, свинец, золото и серебро). Железо может быть в нескольких кристаллических формах с различным расположе-нием атомов. Это явление называется аллотропией.Аллотропические превращения железа наблюдаются при изменении температуры. Железо из расплавленной массы кристаллизуется в форме решетки объемно центрированного куба (рис. 1, 1) – δ – модификация железа; при охлаждении до температуры 1390 °С она перекристаллизовывается в решетку гранецентрированного куба (рис. 1, 2) – γ – модификация железа, а при 898 °С снова образует решетку объемно центрированного куба β и α-модификации. Аллотропия железа имеет большое значение в процессах горячей механической и термической обработки чугуна и стали. Главную роль при этом играют α- и γ-модификации железа. Регулируя закалкой , отжигом и другими способами содержание этих модификаций в сталях, придают им заданные механические свойства.
Кристаллическая природа металлов обуславливает анизотропию их свойств, т.е. различие свойств металлов в зависимости от направления кристаллографических осей, образующих кристаллы металлов.
Процесс перегруппировки атомов в кристаллографической решетке происходит в твердом состоянии металла подобно процессу затвердевания жидкого сплава при определенных- температурах и сопровождается тепловым эффектом. Этот процесс образования новых кристаллов из кристаллов прежней модификации называется вторичной кристаллизацией.
Металлические сплавы, представляющие собой поликристаллические тела, в которых кристаллиты (кристаллические образования, которые при правильном внутреннем строении не сохранили в процессе роста правильную форму кристалла вследствие помех соседних кристаллов) различно ориентированы один относительного другого, обладают мнимой изотропностью (квазии-зотропны). Однако в результате технологической обработки сплава (прокатки, волочения, ковки и т.д.) происходит ориентировка кристаллов по направлению обработки, и металл становится анизотропным. Некоторые механические свойства металлических сплавов при технологической и термической обработках повышаются в направлении главных кристаллографических осей. Этим частопользуются при изготовлении некоторых деталей машин и металлических строительных изделий.
Процесс кристаллизации металлических сплавов начинается при охлаждении жидкого сплава и продолжается у многих сплавов до определенных температур в отвердевшем состоянии в виде перекристаллизации. На размер и форму образующихся кристаллов влияет скорость охлаждения жидкого сплава: при медленном охлаждении образуются крупные зерна, а при быстром – металлический сплав приобретает мелкозернистое строение.
В настоящее время измельчение зерна металла достигается не только за счет увеличения скорости охлаждения, но и за счет введения различных присадок, увеличивающих число центров кристаллизации при V=const и создающих условия для замедленного роста кристаллов. Этот метод измельчения зерна называется модифицированиеми применяется при выплавке специальных чугунов, сталей и некоторых цветных металлов.
Основными способами модифицирования структуры и свойств стали применяемыми в современной металлургии, являются:
– введением в расплавленный металл веществ образующих тугоплавкие соединения, являющиеся центрами кристаллизации (Ti, Al, Si, Mn);
– введение лигирующих элементов, повышающих прочность кристаллических решоток феррита и ацетенита, замедляющих диффузионные процессы выделения углерода, карбидов и движение дислокаций;
– термическая и пормомеханическая обработка.
При затвердевании металлических слитков, болванок, заготовок образуются различные по крупности кристаллы: более мелкие у наружной поверхности, а более крупные внутри слитка. Кроме того, кристаллы ориентированны различно: внутри слитка они имеют более правильные формы, чем в наружных слоях, а чаще всего приобретают разветвленную древовидную форму. Такие скопления кристаллов в слитках называются дендритами.Возможно также образование кристаллов пластинчатой, игольчатой и других форм.
Затвердевание слитка по всему объему происходит не одновременно, поэтому и строение слитка неоднородно. В верхней части, у поверхности слитка, затвердевающего в первую очередь, образуются усадочные раковины, окруженные макро и микропорами.
При ускоренном охлаждении сплава внутри отливки могут образоваться полости – газовые пузыри – за счет газов, не успевших удалиться из металлов.
Подобная неоднородность отливок может привести к снижению их механических свойств.
Соответствующей механической обработкой отливки (давлением, прокаткой) с последующей термической обработкой можно придать волокнистое строение в направлении обработки и уменьшить размер зерен, что улучшает его механические свойства. В жидком состоянии большинство сплавов представляет собой однородный жидкий раствор. При переходе в твердое состояние однородность многих сплавов сохраняется за счет внедрения или замещения атомов в кристаллографической решетке растворителя атомами других более легких элементов.
Структура реальных сплавов в значительной степени отличается от идеального строения кристаллов. В реальном металле всегда имеются нарушения макро- и микроскопического характера (поры, газовые и неметаллические включения, микротрещины и пр.), а также дефекты кристаллического строения, связанные с нарушением правильного расположения атомов в самой кристаллической решетке. Все эти виды нарушений заметно влияют на свойства, причем наиболее велика роль несовершенства кристаллического строения, так называемых дислокаций. Из-за присутствия в металле дислокаций теоретическая прочность не реализуется. Прочность реальных кристаллов обычно составляет не более 1-5% от теоретической, рассчитанной по силам связи между атомами. В конструкции же, когда на эксплуатационные характеристики металла оказывают такие факторы, как наличие надрезов, напряженное состояние, температурные условия эксплуатации, агрессивность окружающей среды, используется только от 40 до 80% прочности исходного металла.
Член – корреспондент АНСССР И. А. Одинг еще в конце 40х годов прошлого столетия, сформулировал основные закономерности изменения прочности кристаллических тел в зависимости от от плотности дислокаций, благодаря им получили интенсивное развитие:
1. получение металлов с кристаллическим строением близким к совершенству (создание бездислакационных кристаллов с прочностью приближающейся к теоретической), и разработка на этой основе высокопрочных композиционных материалов;
2. создание в уже имеющихся материалах повышенной или высокой плотности дислокаций, что при условии равномерного или периодического распределения в объеме металла позволяет в несколько раз повысить его прочность;
Во втором пути повышения прочности металлов используются два основных метода:
– пластическая деформация (механическая энергия) для достижения необходимой плотности дислокаций;
– термическое воздействие (тепловая энергия).
Наиболее эффективно повышает прочность комбинация этих двух способов с названием термомеханическая обработка (ТМО).
Влияние структурных составляющих на свойства железоуглеродистых сплавов
Основными структурными составляющими железоуглеродистых сплавов является графит, феррит, цементит, аустенит, ледебурит и перлит, обладающие различными свойствами; поэтому количественное содержание их сильно влияет на свойства железоуглеродистых сплавов.
Графит– мягок, его истинная плотность 2,25 г/см 3 , он нарушает сплошность металла, понижая сопротивление растяжению и вязкость, увеличивает хрупкость тем больше, чем крупнее его частицы. Графит характеризует микроструктуру литейных чугунов.
Феррит– твердый раствор углерода в aFe, мягкий, вязкий, хорошо куется и сваривается. Чем больше в металле феррита, тем металл мягче, более ковок и тем больше дает удлинение при растяжении.
Цементит– карбид железа Fe3C. С увеличением его содержания сначала возрастают твердость и прочность металла (наибольший предел прочности при растяжении – при содержании углерода 1,2%); с дальнейшим увеличением количества цементита сопротивление падает, вязкость уменьшается, а твердость и хрупкость возрастает.
Аустенит– твердый раствор углерода в γ Fе; содержит до 2% углерода. В обыкновенных сталях аустенит устойчив только при температуре выше 723°С В легированных сталях, содержащих в своем составе некоторое количество Мп, Cr, Ni и других элементов, аустенит может быть устойчивым и при обычной, и даже низкой температуре. Механические свойства аустенита зависят от содержания в нем углерода. С уменьшением количества углерода аустенит становится более мягким и вязким; с увеличением – более твердым и хрупким.
Ледебурит– эвтетика (цементит + аустенит), очень тверд и хрупок, присутствует в белых чугунах. Образуется при температуре 1130 °С и содержит углерода С=4,3% – эвтектический чугун.
Перлит– эвтектоид (феррит + цементит), обладает сравнительно высокой прочностью, достаточно вязок, имеет зернистое или пластинчатоестроение. Образуется в процессе распада аустенита при температуре 723°C и содержанием углерода 00,83%, примеси Si, Мпспособствуют образованию перлита и при меньшем содержании углерода.
Не нашли то, что искали? Воспользуйтесь поиском: