Ювелирное обозрение
Все о ювелирных украшениях, драгоценных камнях и металлах
Кальцинированная сода это какая
Содержание
Сода и ее разновидности известны давно. Люди еще в древности узнали о свойствах этих природных веществ и стали пользоваться ими для своих нужд.
В наши дни кальцинированная сода успешно используется во многих видах промышленности и в домашних условиях.
Отличие кальцинированной соды
Из всех видов соды самая известная — пищевая. Ее добавляют в тесто для пышности, в кислые блюда для уменьшения кислотности. Пищевой содой полощут горло, лечат изжогу и другие заболевания.
В отличие от пищевой, другие виды соды не употребляются в пищу и в качестве медицинского средства
Применение кальцинированной и каустической соды требует определенной осторожности. Каустическая химически активна и вызывает серьезные ожоги, поэтому ей обычно не пользуются дома.

Кальцинированную соду применяют при отстирывании сильных загрязнений и въевшихся пятен. Никогда не забывайте, что, хотя формулы разных типов соды очень похожи, это вещества с разными характеристиками.
Важно знать о кальцинированной соде:
- кальцинированную соду держать отдельно от еды;
- хранить в местах, недоступных для детей;
- плотно закрывать, название сохранить.
Что представляет собой кальцинированная сода
Научное название кальцинированной соды — карбонат натрия Na2CO3. Для сравнения, формула пищевой соды -NaHCO3.
Входит в состав природных ископаемых. При выделении из минералов имеет вид бесцветных кристаллов разного размера.
Как полезное ископаемое сода добывается из содовых озер. Месторождения есть в Сибири и в Забайкалье. Наряду с природной содой, в промышленности используется кальцинированная сода, полученная на производстве.

Виды кальцинированной соды и способы ее использования
Использование кальцинированной соды в промышленности
В промышленных масштабах применяется кальцинированную соду подразделяют на марки А и Б.
Сода высшего сорта марки А используется в производстве особого вида стекла. Кальцинированная сода высшей пробы отличается строгими требованиями к механическому составу вещества, то есть к размеру кристаллов.
Сода марки Б не отличается по химическому составу, но не имеет ограничений по размеру кристаллов. Она входит в состав многих стиральных порошков, отбеливателей, других моющих средств. Также она применяется в химической промышленности в производстве глицеринов, некоторых спиртов, в производстве краски, бумаги, целлюлозы, в нефтеперерабатывающей промышленности. С помощью кальцинированной соды производят еще один вид соды — каустическую. Кроме того, кальцинированную соду используют в фармацевтической промышленности для синтеза некоторых лекарственных препаратов.

Польза и вред кальцинированной соды при использовании в быту
Учитывая полезные свойства кальцинированной соды, в домашнем хозяйстве ее обычно применяют:
- для удаления жирных пятен с белья и одежды;
- для удаления пятен краски с различных поверхностей;
- для чистки посуды, кухонных поверхностей, сантехники;
- для ликвидации засоров в канализационных трубах;
- для смягчения воды при стирке;
- для защиты деталей стиральной машины от накипи;
- вместо стирального порошка для стирки вещей;
- в садово-огородных работах;
- для дезинфекции.
Неправильное использование кальцинированной соды может привести к неприятностям. Если перепутать кальцинированную соду с пищевой, можно нанести вред своему здоровью.
Если использовать кальцинированную соду для стирки и выведения пятен с одежды, надо учитывать, что она не подходит для деликатных вещей из шелка, тонкого атласа и шерсти. Для таких вещей пользуйтесь мылом или специальными стиральными порошками для деликатных вещей и шерсти. Если Вы не знаете точно состав ткани, которую собираетесь постирать кальцинированной содой, протестируйте на кусочке ткани или на отвороте шва с изнанки вещи.

Применение кальцинированной соды на садово-огородном участке
Садоводы взяли на вооружение, что кальцинированная сода — эффективный помощник в борьбе с самыми распространенными вредителями — серой гнилью, гусеницами и некоторыми другими.
Если Вы пользуетесь готовым средством для борьбы с вредителями, точно следуйте инструкции, чтобы не навредить растениям и будущему урожаю.
Для самостоятельного приготовления рекомендуется приготовить раствор: 3-4 столовые ложки кальцинированной соды на ведро воды.
Если концентрация карбоната натрия (кальцинированной соды) в почве будет превышена, нарушатся процессы обмена веществ. Растения могут заболевать и не давать урожая.
Сегодня кальцинированная сода применяется во многих отраслях промышленности и в домашнем хозяйстве.
Сода — общее название технических натриевых солей угольной кислоты.
- Na2CO3 (карбонат натрия) — кальцинированная сода
- Na2CO3·10H2O (декагидрат карбоната натрия, содержит 62,5% кристаллизационной воды) — кристаллическая сода; иногда выпускается в виде Na2CO3·H2O или Na2CO3·7H2O
- NaHCO3 (гидрокарбонат натрия) — питьевая или пищевая сода, натрий двууглекислый, бикарбонат натрия
Название «сода» происходит от растения Salsola Soda, из золы которого её добывали. Кальцинированной соду называли потому, что для получения её из кристаллогидрата приходилось его кальцинировать (то есть нагревать до высокой температуры).
Каустической содой называют гидроксид натрия (NaOH).
Оксиды и гидроксиды
| Вид | Для Na | Для С |
|---|---|---|
| Гидроксид | NaOH | H2CO3 |
| Оксид | Na2O | CO2 |
Нахождение в природе
В природе сода встречается в золе некоторых морских водорослей, а также в виде следующих минералов:
Современные содовые озёра известны в Забайкалье и в Западной Сибири; большой известностью пользуется озеро Натрон в Танзании и озеро Сирлс в Калифорнии. Трона, имеющая промышленное значение, открыта в 1938 в составе эоценовой толщи Грин-Ривер (Вайоминг, США). Вместе с троной в этой осадочной толще обнаружено много, ранее считавшихся редкими, минералов, в том числе давсонит, который рассматривается как сырьё для получения соды и глинозёма. В США природная сода удовлетворяет более 40% потребности страны в этом полезном ископаемом. В России из-за отсутствия крупных месторождений сода из минералов не добывается.
Получение
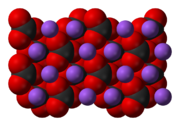
До начала XIX века карбонат натрия получали преимущественно из золы некоторых морских водорослей и прибрежных растений.
Способ Леблана
В 1791 году французский химик Никола Леблана получил патент на «Способ превращения глауберовой соли в соду». По этому способу при температуре около 1000°C запекается смесь сульфата натрия («глауберовой соли»), мела или известняка (карбоната кальция) и древесного угля. Уголь восстанавливает сульфат натрия до сульфида:
Сульфид натрия реагирует с карбонатом кальция:
Полученный расплав обрабатывают водой, при этом карбонат натрия переходит в раствор, сульфид кальция отфильтровывают, затем раствор карбоната натрия упаривают. Сырую соду очищают перекристаллизацией. Процесс Леблана даёт соду в виде кристаллогидрата (см. выше), поэтому полученную соду обезвоживают кальцинированием.
Сульфат натрия получали обработкой каменной соли (хлорида натрия) серной кислотой:
Выделявшийся в ходе реакции хлороводород улавливали водой с получением соляной кислоты.
Первый содовый завод такого типа в России был основан промышленником М. Прангом и появился в Барнауле в 1864 году.
После появления более экономичного (не остаётся в больших количествах побочный сульфид кальция) и технологичного способа Сольве, заводы, работающие по способу Леблана, стали закрываться. К 1900 90% предприятий производили соду по методу Сольве, а последние фабрики, работающие по методу Леблана закрылись в начале 1920-х.
Промышленный аммиачный способ (способ Сольве)
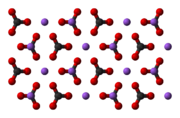
В 1861 году бельгийский инженер-химик Эрнест Сольве запатентовал метод производства соды, который используется и по сей день.
В насыщенный раствор хлорида натрия пропускают эквимолярные количества газообразных аммиака и диоксида углерода, то есть как бы вводят гидрокарбонат аммония NH4HCO3:
Выпавший остаток малорастворимого (9,6 г на 100 г воды при 20°C) гидрокарбоната натрия отфильтровывают и кальцинируют (обезвоживают) нагреванием до 140—160°C, при этом он переходит в карбонат натрия:
Образовавшийся диоксид углерода и аммиак, выделенный из маточного раствора на первой стадии процесса по реакции:
возвращают в производственный цикл.
Первый содовый завод такого типа в мире был открыт в 1863 в Бельгии; первый завод такого типа в России был основан в районе уральского поселка Березники фирмой «Любимов, Сольве и Ко» в 1883 году. Его производительность составляла 20 тысяч тонн соды в год.
До сих пор этот способ остаётся основным способом получения соды во всех странах.
Способ Хоу
Разработан китайским химиком Хоу (Hou Debang) в 1930-х годах. Отличается от процесса Сольве тем, что не использует карбонат кальция.
По способу Хоу в раствор хлорида натрия при температуре 40 градусов подается диоксид углерода и аммиак. Менее растворимый гидрокарбонат натрия в ходе реакции выпадает в осадок (как и в методе Сольве). Затем раствор охлаждают до 10 градусов. При этом выпадает в осадок хлорид аммония, а раствор используют повторно для производства следующих порций соды.
В настоящее время в ряде стран практически весь искусственно производящийся карбонат натрия вырабатывается по методу Хоу.
Свойства
Кристаллогидраты карбоната натрия существуют в разных формах: бесцветный моноклинный Na2CO3·10H2O, при 32,017°С переходит в бесцветный ромбический Na2CO3·7H2O, последний при нагревании до 35,27°C бесцветный переходит в ромбический Na2CO3·H2O.
Безводный карбонат натрия представляет собой бесцветный кристаллический порошок.
| Параметр | Безводный карбонат натрия | Декагидрат Na2CO3·10H2O |
|---|---|---|
| Молекулярная масса | 105,99 а.е.м. | 286,14 а.е.м. |
| Температура плавления | 852°C (по другим источникам, 853°C) | 32°С |
| Растворимость | Не растворим в ацетоне, и сероуглероде, мало растворим в этаноле хорошо растворим в глицерине, и воде (см. таблицу ниже) | растворим в воде, не растворим в этаноле |
| Плотность ρ | 2,53 г/см 3 (при 20°C) | 1,446 г/см 3 (при 17°C) |
| Стандартная энтальпия образования ΔH | −1131 кДж/моль (т) (при 297 К) | −4083,5 кДж/моль ((т) (при 297 К) |
| Стандартная энергия Гиббса образования G | −1047,5 кДж/моль (т) (при 297 К) | −3242,3 кДж/моль ((т) (при 297 К) |
| Стандартная энтропия образования S | 136,4 Дж/моль·K (т) (при 297 К) | |
| Стандартная мольная теплоёмкость Cp | 109,2 Дж/моль·K (жг) (при 297 К) |
| Температура, °C | 10 | 20 | 25 | 30 | 40 | 50 | 60 | 80 | 100 | 120 | 140 | |
| Растворимость, г Na2CO3 на 100 г H2O | 7 | 12,2 | 21,8 | 29,4 | 39,7 | 48,8 | 47,3 | 46,4 | 45,1 | 44,7 | 42,7 | 39,3 |
В водном растворе карбонат натрия гидролизуется, что обеспечивает щелочную реакцию среды. Уравнение гидролиза (в ионной форме):
Первая константа диссоциации угольной кислоты равна 4,5·10 -7 . Все кислоты, более сильные, чем угольная, вытесняют её в реакции с карбонатом натрия. Так как угольная кислота крайне нестойкая, она тут же разлагается на воду и углекислый газ:
Применение
Карбонат натрия используют в стекольном производстве, мыловарении и производстве синтетических моющих средств, эмалей, для получения ультрамарина. Также он применяется для умягчения воды паровых котлов и вообще устранения жёсткости воды, для обезжиривания металлов и десульфатизации доменного чугуна. Карбонат натрия — исходный продукт для получения NaOH, Na2B4O7, Na2HPO4.
В пищевой промышленности зарегистрирован в качестве пищевой добавки E500, регулятора кислотности, разрыхлителя, препятствующего комкованию и слёживанию.[1]
Ссылки
Разное: Воск (E900-909) • Глазурь (E910-919) • Восстановитель (E920-929) • Газ для упаковки (E930-949) • Заменители сахара (E950-969) • Вспениватель (E990-999)
Wikimedia Foundation . 2010 .
Смотреть что такое "Кальцинированная сода" в других словарях:
КАЛЬЦИНИРОВАННАЯ СОДА — то же, что карбонат натрия Na2CO3; см. Сода … Большой Энциклопедический словарь
Кальцинированная сода — более слабое щелочное средство в сравнении с едким натром. Представляет собой белый мелкокристаллический порошок, хорошо растворимый в воде. Горячие растворы кальцинированной соды хорошо омыляют жиры и гидролизуют белки. Источник: Санитарные… … Официальная терминология
кальцинированная сода — то же, что карбонат натрия Na2CO3; см. сода. * * * КАЛЬЦИНИРОВАННАЯ СОДА КАЛЬЦИНИРОВАННАЯ СОДА, то же, что карбонат натрия Na2CO3; см. Сода (см. СОДА) … Энциклопедический словарь
кальцинированная сода — natrio karbonatas statusas T sritis chemija formulė Na₂CO₃ atitikmenys: angl. calcined soda; soda ash; sodium carbonate rus. кальцинированная сода; натрий углекислый; натрия карбонат ryšiai: sinonimas – dinatrio trioksokarbonatas sinonimas –… … Chemijos terminų aiškinamasis žodynas
Кальцинированная сода — то же, что Натрия карбонат Na2CO3; см. также Сода … Большая советская энциклопедия
КАЛЬЦИНИРОВАННАЯ СОДА — то же, что карбонат натрия Nа2СОз; см. Сода … Естествознание. Энциклопедический словарь
КАЛЬЦИНИРОВАННАЯ СОДА — смотри Сода … Металлургический словарь
КАЛЬЦИНИРОВАННАЯ СОДА — кальцинированная сода, см. Натрия карбонат … Ветеринарный энциклопедический словарь
Блог о домашнем хозяйстве, организации пространства, хранении вещей, о чистоте и порядке, о семье и здоровье, а также DIY.
Страницы
8 мая 2019 г.
Сода: пищевая, кальцинированная и каустическая.

ПИЩЕВАЯ СОДА.
Историческая справка.
Пищевая сода на сегодняшний день – продукт химического производства. Но известна она была задолго до того, как ее научились получать искусственным путем. Еще древние египтяне пользовались ей в качестве мыла. Добывалась сода из озер и других месторождений. Я читала, что содовые озера есть и у нас в Забайкалье и Сибири. Но в целом эти месторождения невелики, поэтому искусственные способы получения соды на первом месте. Большие месторождения соды есть в США.
 |
| Содовые озера. В Кулундинскои степи такие озера называют "бельевыми". Местные жители до сих пор приезжают на такие озера для стирки белья без мыла. Наибольшую известность в нашей стране получили содовые озера на юге Западной и Восточной Сибири. Особенно знамениты Михайловско-Петуховские содовые озера в Кулундинскои степи. Они являются основными поставщиками природной соды. |
| Фото из свободного доступа в сети. |
Впервые сода была получена химическим путем в 1791 году французом Лебланом, именно этот факт позволил французской выпечке занять лидирующие позиции. Потому и рецепт получения соды долгое время держался в строжайшей тайне и был достоянием Франции.

- Антисептик.
- Нейтрализует кислоту.
- Обладает хорошими чистящими характеристиками.
- Смягчает воду.
- Очень многие, и я в том числе, используют пищевую соду в медицинских целях. Сильно вдаваться в подробности не буду, поскольку так на целую книгу можно размахнуться, но раствор соды или содовая кашица, и правда, отличный помощник для поддержания здоровья:
- для полоскания горла при лор-заболеваниях,
- для обработки и подсушивания ран,
- в комплексе противогрибкового лечения
- в качестве противозудного и противовоспалительного средства
- отлично убирает запах изо рта при полоскании, а также отбеливает зубы (но вот чистить зубы абразивом и часто я бы не стала)
- спасет от изжоги;
- . ставлю многоточие, так как список может быть сильно продолжен.
Важный нюанс. Для внутреннего применения содовый раствор должен быть не холодным, а слегка горячим, приблизительно 60 градусов, именно при такой температуре идет необходимый распад соды на карбонат натрия, углекислый газ и воду.
2. Для поддержания красоты. Сода отличное составляющее для всевозможных масок, скрабов для лица, которые и прыщам дадут отпор, и состояние кожи улучшат.
Пол чайной ложки пищевой соды + пол чайной ложки мелкой соли + одна столовая ложка кефира. Нанести на лицо и АККУРАТНО (без фанатизма) массировать. И отшелушивает хорошо, и смягчает, и антибактериальный эффект присутствует. Долго на лице держать не следует, может быть аллергическая реакция или даже ожог. Минут 5 пиллинга, а после смыть и воспользоваться увлажняющим или питательным кремом. Такое скрабирование кожи достаточно делать раз в неделю, чаще не надо.
В чайную ложку соды добавить несколько капель геля для умывания или жидкого мыла. Помассировать и смыть.
КАЛЬЦИНИРОВАННАЯ СОДА.


Что важно знать о кальцинированной соде, чтобы использовать ее эффективно?
Смешать кальцинированную и пищевую соду (1:1), развести теплой водой до состояния кашицы нанести на поверхность и оставить на полчаса, после вымыть горячей водой.
Универсальный содовый раствор. На стакан кипятка – 1 столовая ложки соды, тщательно размешать до полного растворения и перелить в бутылку с распылителем. Никаких точных пропорций для таких растворов нет, чем сильнее въелась грязь, чем она устойчивее к мытью, тем концентрированнее можно сделать раствор, а еще можно добавить обычное моющее средство для посуды. И желательно при использовании давать средству время для воздействия: обильно нанесли, оставили минут на 15, смыли горячей водой. Эта щелочь не подходит для капризных поверхностей, только для тех, что и хлорку бы выдержали. Например, кафель, рабочая кухонная поверхность, плита, духовка, сантехника, линолеум… Также нельзя использовать для тефлоновых покрытий, алюминиевой и чугунной посуды.
